时代投研 | 2020医改政策趋势分析报告:三医联动顶层设计,催创新强监管并举
2015年以来,医药行业自上而下推行新一轮系统化的监管改革和政策改革,从监管机构的顶层设计,到产业链上下游都做了较大的调整,政策发布主体涵盖国务院、卫健委、人社部、药监局、财政部、发改委、商务部等多个中央部门和省级地市级的相关监管机构。政策发布数量以万份计,仅其中单一年份的国家级发布文件都在300份以上。
时代商学院特约研究员 雷小艳
2015年以来,医药行业自上而下推行新一轮系统化的监管改革和政策改革,从监管机构的顶层设计,到产业链上下游都做了较大的调整,政策发布主体涵盖国务院、卫健委、人社部、药监局、财政部、发改委、商务部等多个中央部门和省级地市级的相关监管机构。政策发布数量以万份计,仅其中单一年份的国家级发布文件都在300份以上。
本报告将梳理与分析近年来的重点政策、政策效果,并对未来的政策动向进行展望。
1.三医联动:顶层机构设置与总体思路
总体来说,改革分为四条主线。
第一,在监管机构设置上,新设立医保局,调整药监局、卫健委部分权责,并以医保局牵头药监局、卫健委,形成医保、医药、医疗三医联动的监管机制;
第二,在三医联动监管机制和医保支付压力下,对医药端落地一致性评价,流通端落地两票制,医保局作为战略购买者推动集中采购下的药品支付价格重塑和医保多元化支付方式落地,以达到优化医保用药结构和医保控费效果。
第三,引导产业创新升级,提高创新药研发的审评审批效率,提高进口新药上市国内市场的审批效率,医保目录改为一年一次的动态调整,缩短新药进入医保的时间周期,推动创新药研发行业的专业化分工,CRO(医药研发外包)、CMO(医药生产外包)等新兴子行业得到快速发展。
第四,提高医药行业服务能力,驱动医疗资源下沉基层,落地分级诊疗和医联体建设,鼓励社会办医,鼓励运用互联网技术实现远程医疗,明确驱动医药分离。
2.专业化分工
那么,医保局、药监局、卫健委如何具体分工和协作来实现畅通的三医联动?
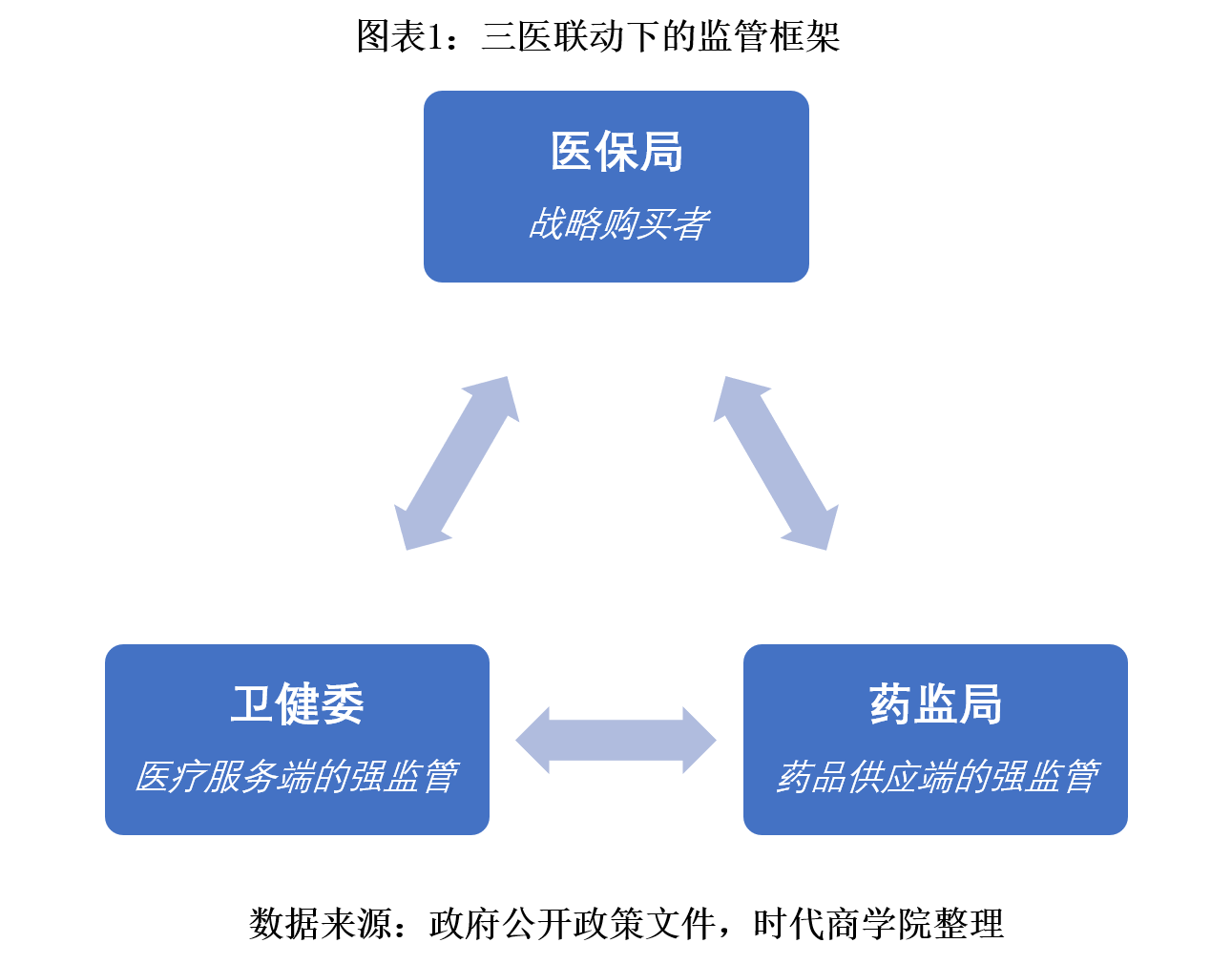
(2)药监局:供应端监管者
作为国家市场监督管理总局直属机构,药监局专门负责药品供应端的全流程监管,从药品研发、生产、流动、疗效再评价、上市后用药事故监测上报等全流程管理保证药品质量和药品供应。
(3)卫健委:服务端监管者
卫健委也是国务院直属机构,在保留原卫计委、老龄办等相关主体职责基础上,集中于医疗服务端的监管,组织制定国家基本药物制度,推进深化医药卫生体制改革,监督管理公共卫生、医疗服务、卫生应急,负责计划生育管理和服务工作,拟定应对人口老龄化、医养结合政策措施等。
自本轮改革以来,卫健委逐步推动公立医院改革,落地药品零加成政策,推进医药分离,推动落地分级诊疗体制建设,城市医共医联体和县域医联体建设也正在加速推进。
3.政策效果分析
(1)一致性评价+集采落地:用药结构优化,降价效果明显
三医联动对医药行业影响最大的是针对仿制药的一致性评价。首先,所有的仿制药企业要面临过不过一致性评价的选择,如果选择不做一致性评价,则相当于从长期来说直接放弃该药品品种,逐步退出市场。对于已经过了一致性评价的品种,则可以视同与原研药同等质量和疗效,在后续医保采购的技术评标环节直接与原研药同台竞价,有望实现对原研药的替代。
对于单一品种而言,政策规定,自第一家品种通过一致性评价后,3年后不再受理其他药品生产企业相同品种的一致性评价申请;同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的生产企业。从这个角度看,一致性评价就是制药行业供给侧改革和集中度提升的有力驱动,推动整个仿制药行业完成质量升级和供应格局优化。
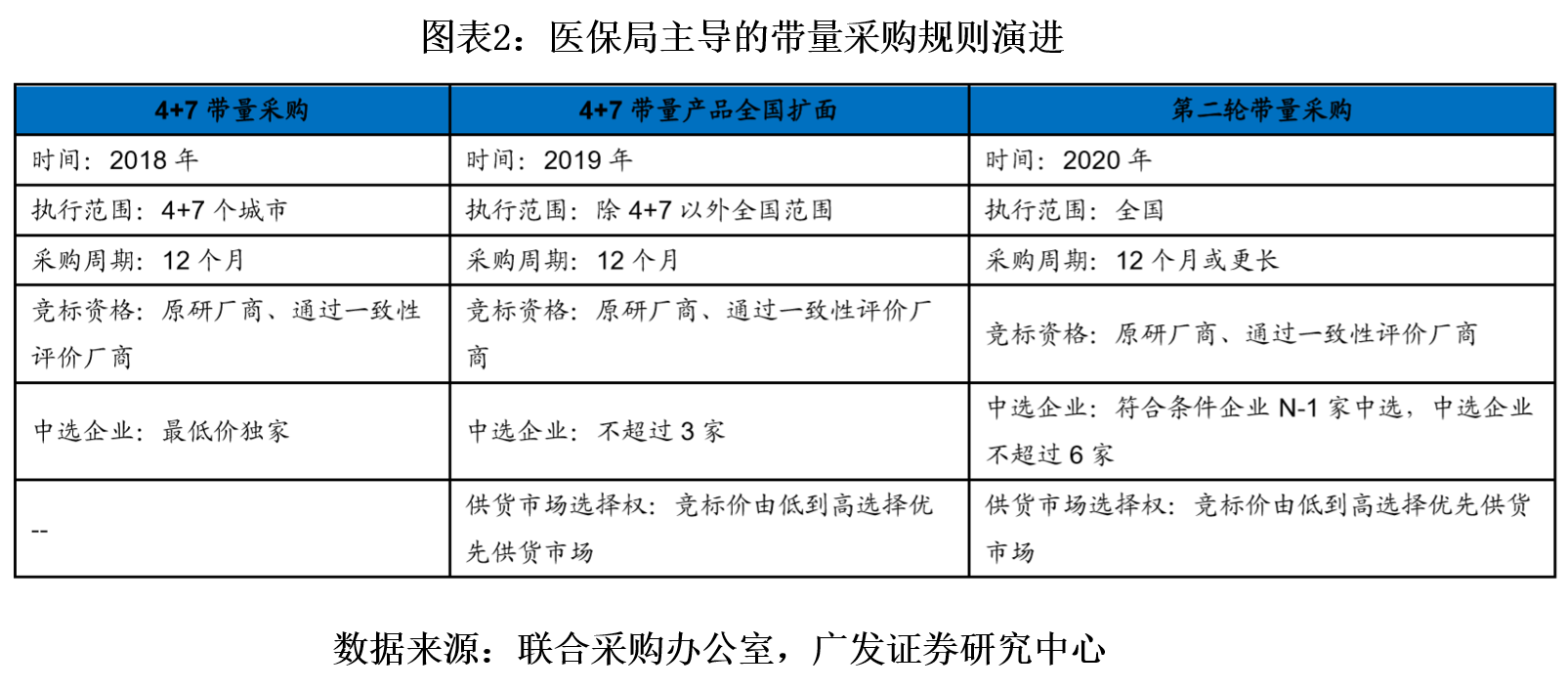
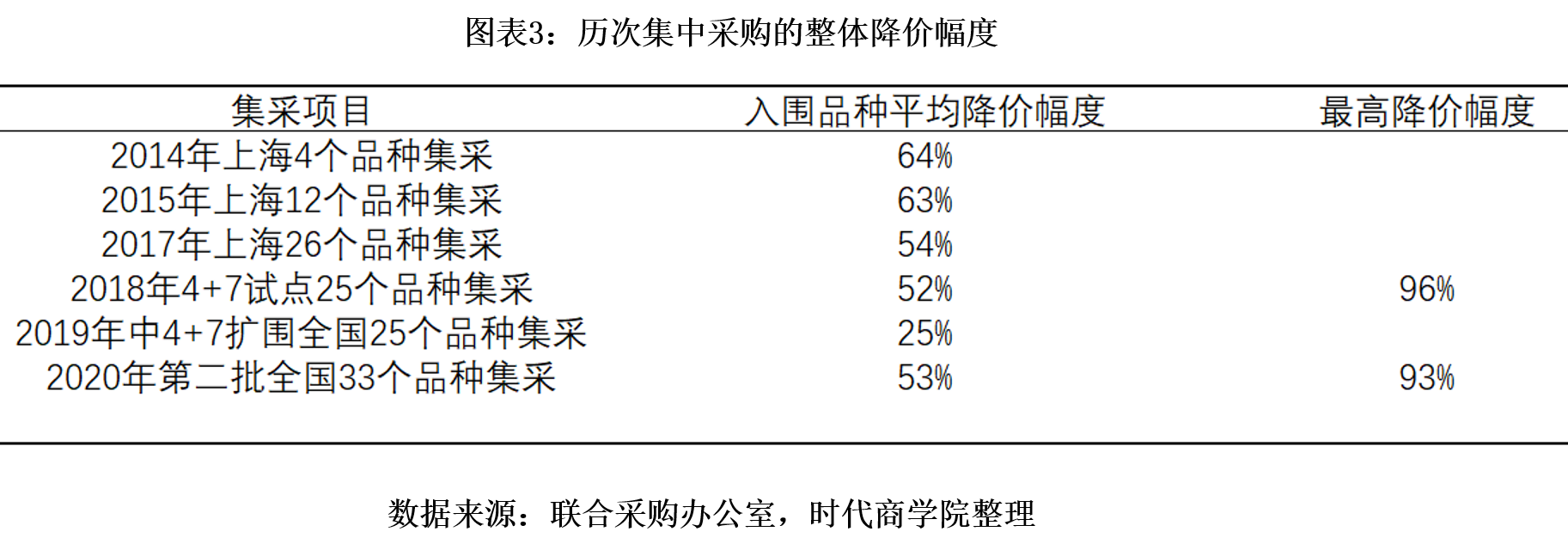
(2)激励环境形成,创新热潮凸显
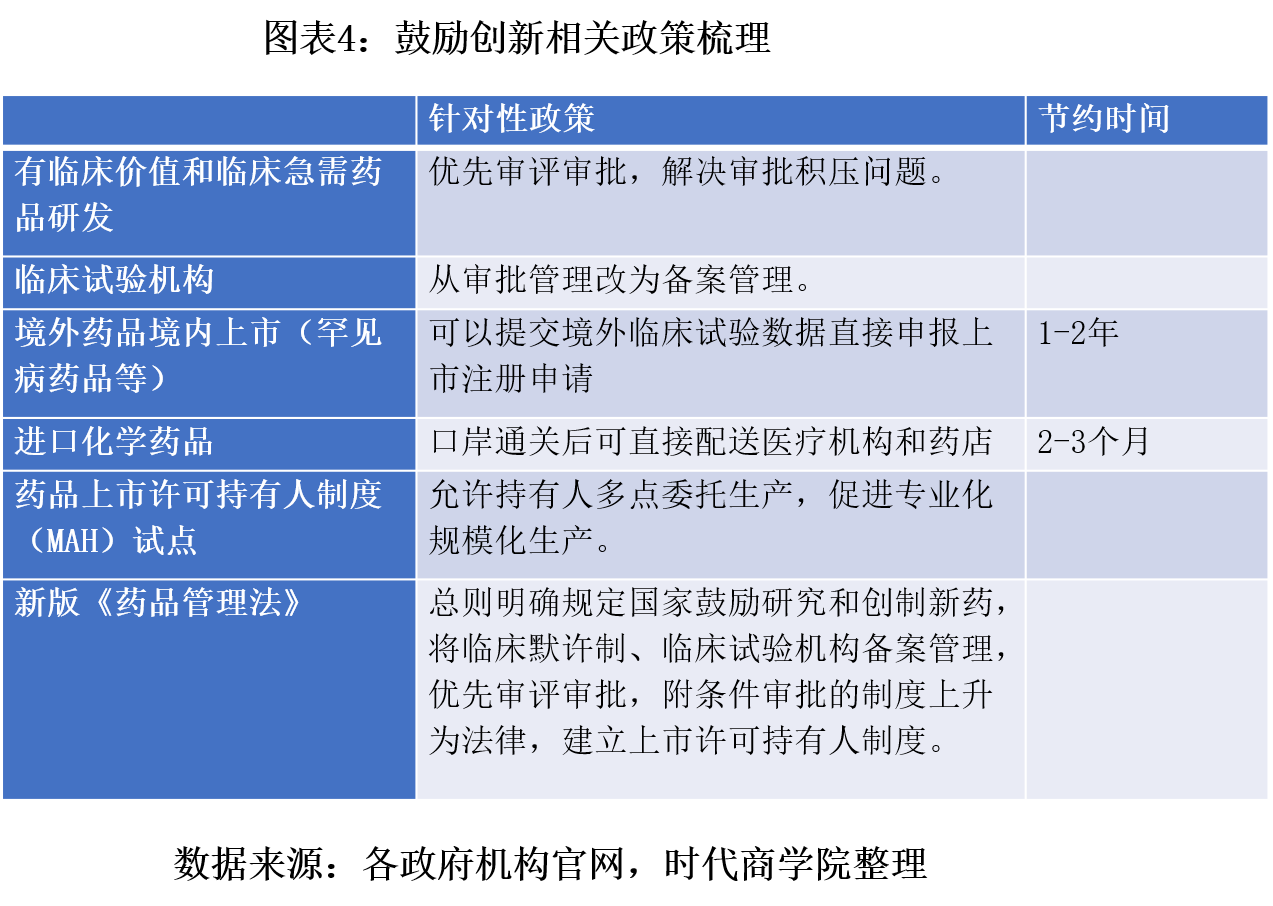
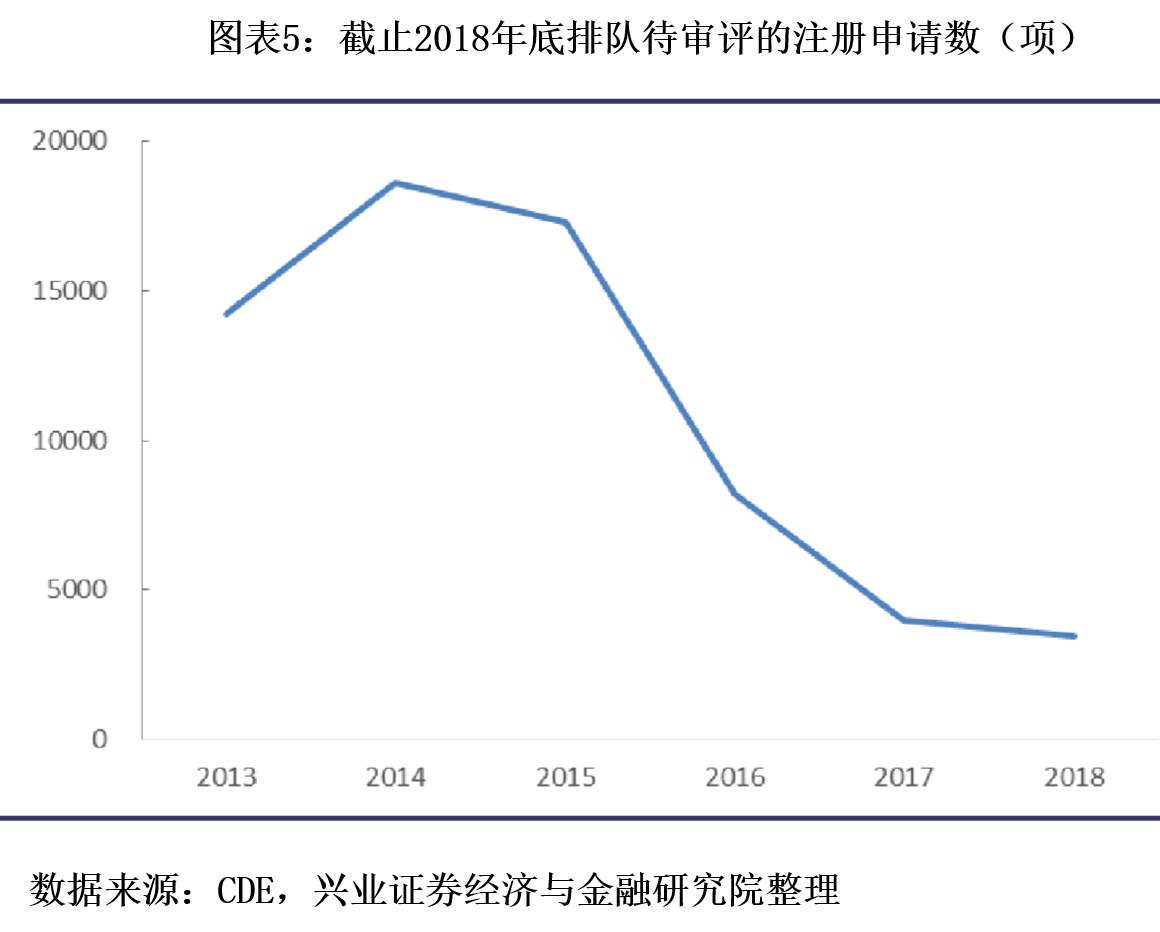
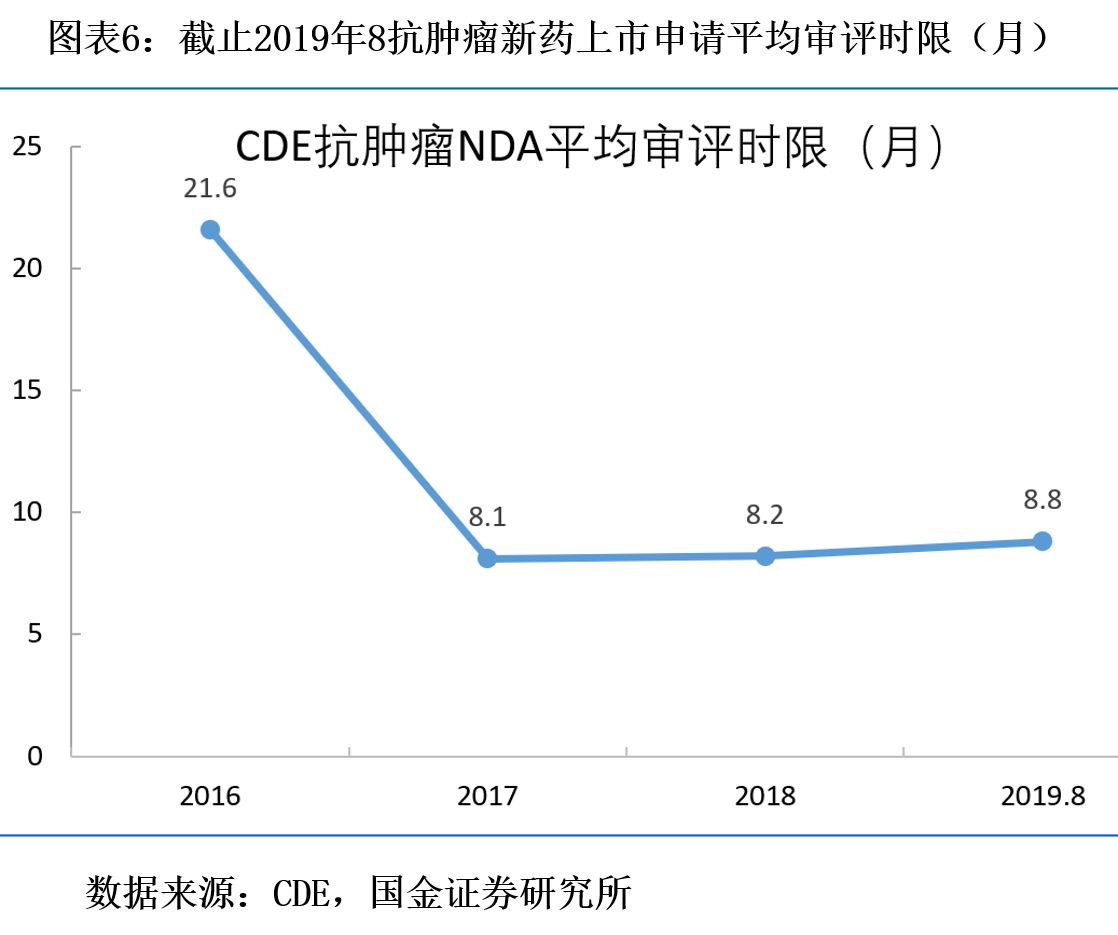
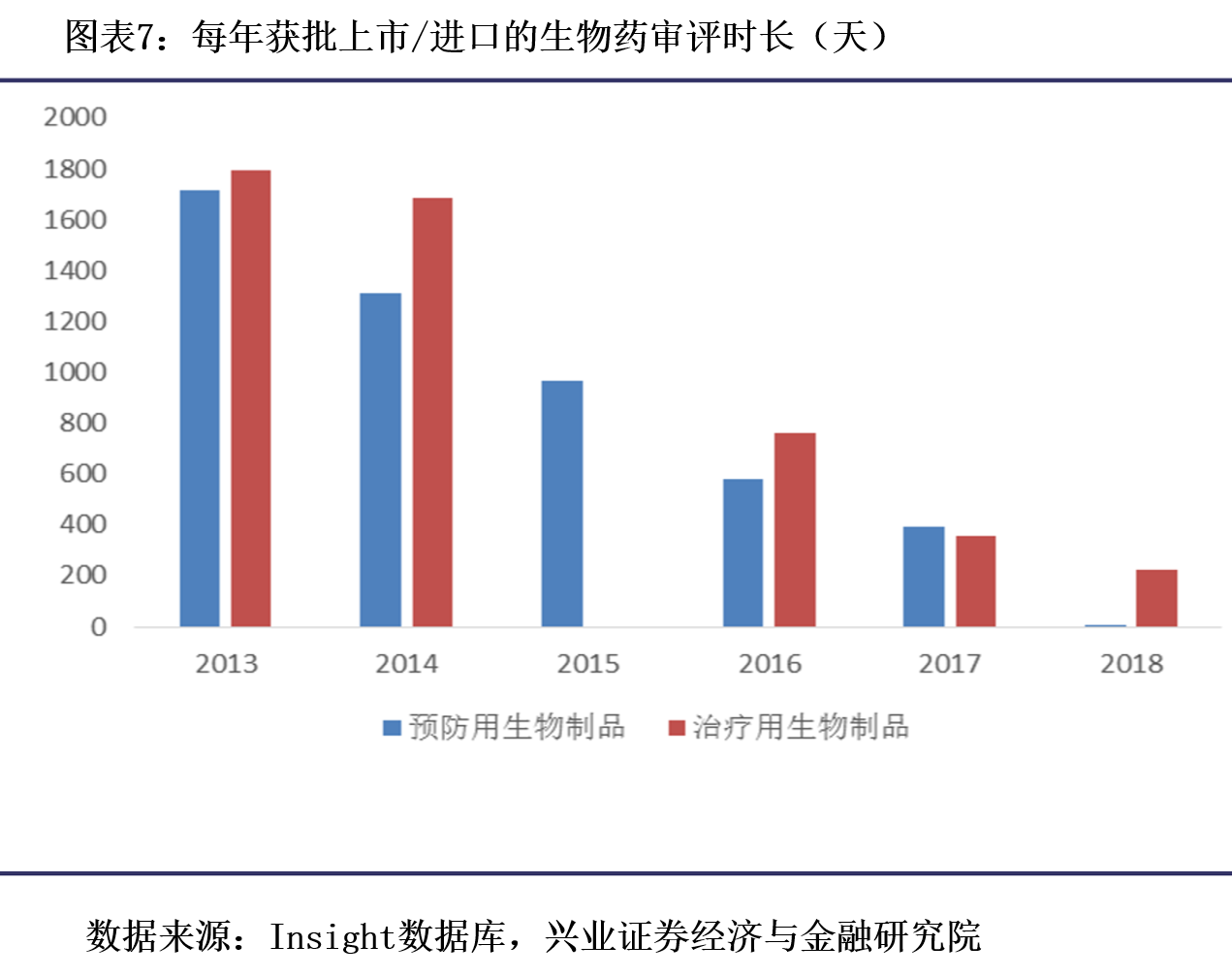
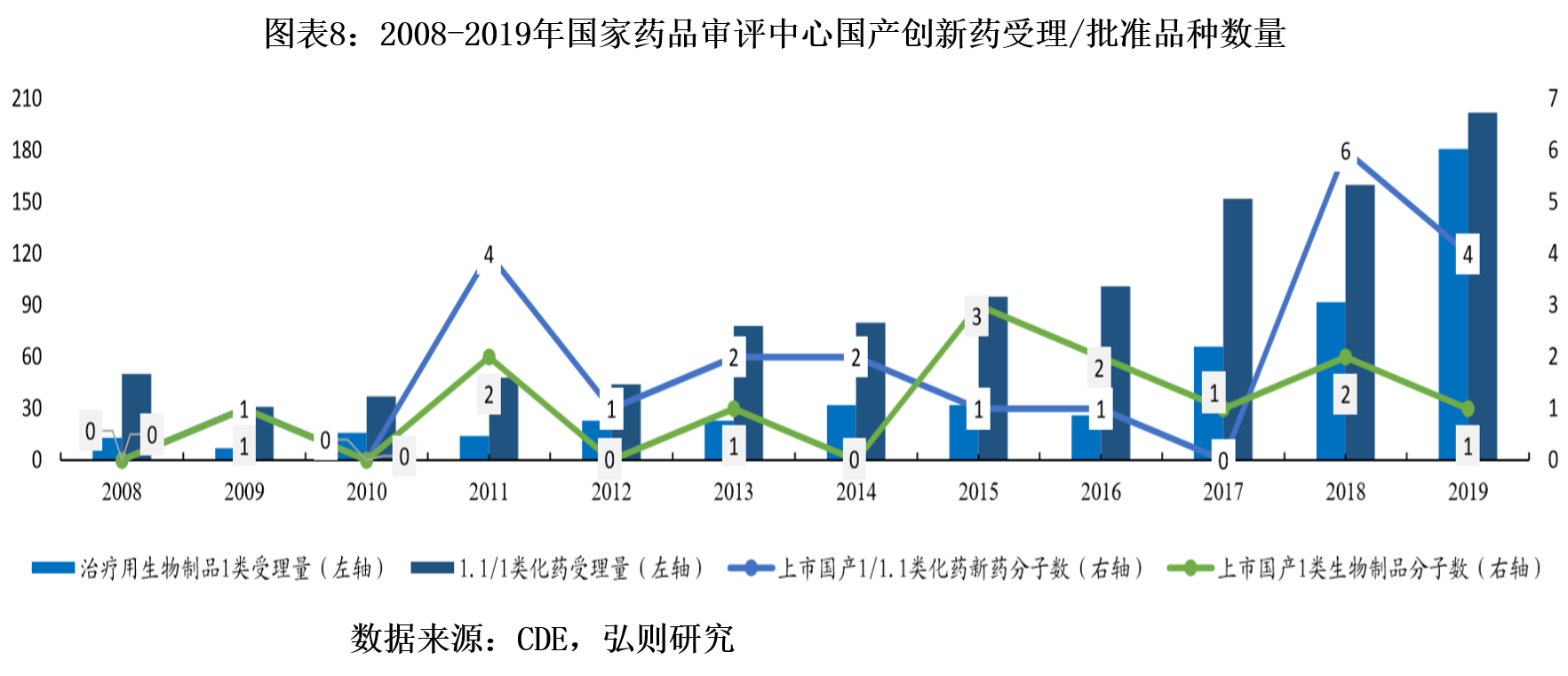
最后,在上市新药销售环节,医保目录改为一年一次的动态调整,新上市的创新药有机会快速进入医保目录,从而实现医保支付范围内的销售放量。而历史上医保目录每隔四五年甚至六七年才调整一次,上市新药只能被动等到目录调整的机会。2017年-2019年医保目录动态调整都及时纳入有临床价值的新药,尤其是2018年-2019年,新上市新药都能在次一年甚至当年实现入医保目录。
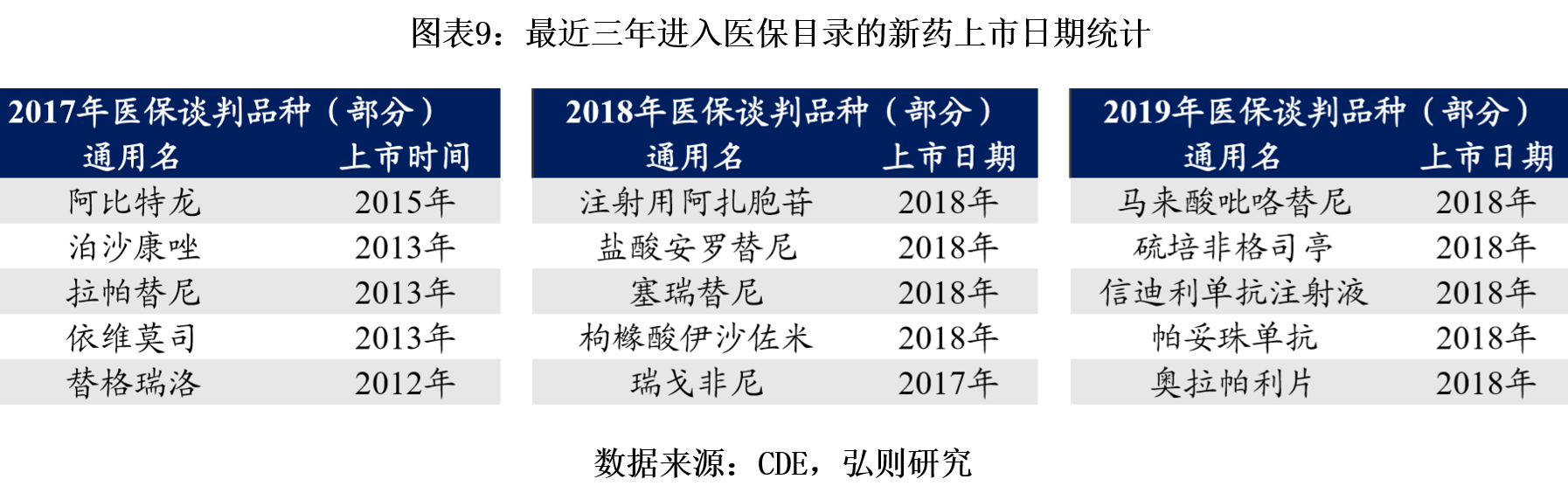
4.政策展望
(1)医保局:集采扩围扩品种,继续推进医保支付方式试点
展望2020年的医药政策趋势,医保局在促降价、防滥用、严监管、助发展的总体思路下,仍然会随着仿制药一致性评价的进度,扩大集采的品种覆盖,同时也会考虑高值耗材等其他采购品类的集中采购政策试点。同时,将继续推进医保支付方式改革,按病种付费、按人头付费、按单元付费都多元化支付方式组合将综合实现医保的合理控费。此外,医保目录动态调整将紧跟研发前沿,提高用药结构优化的速度和效率,切切实实让老百姓用上既有治疗价值,性价比又高的药品。
(2)药监局:注射剂一致性评价将落地
药监局将在深化药审改革、强化药品监管、加强产品全生命周期管理等方面继续深入,在创新药研发的良好制度环境基础上引导产业升级,加快审评审批,出台临床急需境外新药目录引导产业研发方向,加快境内外抗癌新药注册审批和上市节奏,推动临床急需抗癌新药的仿制药替代。按照新版《药品管理法》完善药品全生命周期管理,严控质量标准和药品安全底线。此外,仿制药一致性评价步入正轨之后将继续加速落地注射剂一致性评价。
(3)分级诊疗体系建设加码
卫健委将从提高医疗体系整体服务质量和服务效率角度,继续加强基层医疗建设,加强分级诊疗体系建设,引导终端合理用药,加快公立医院改革和医药分离,从数据监管角度促进三医联动顺畅、引导合理产药和用药。

(4)多方监管
在医药行业上市公司监管方面,2019年6月财政部下发通知对77家药企开展会计信息质量专项检查,其中不乏各个子行业的上市公司。同时,从交易所2019年对医药行业的监管动向看,企业经营质量和诚信度也将继续成为监管重点。
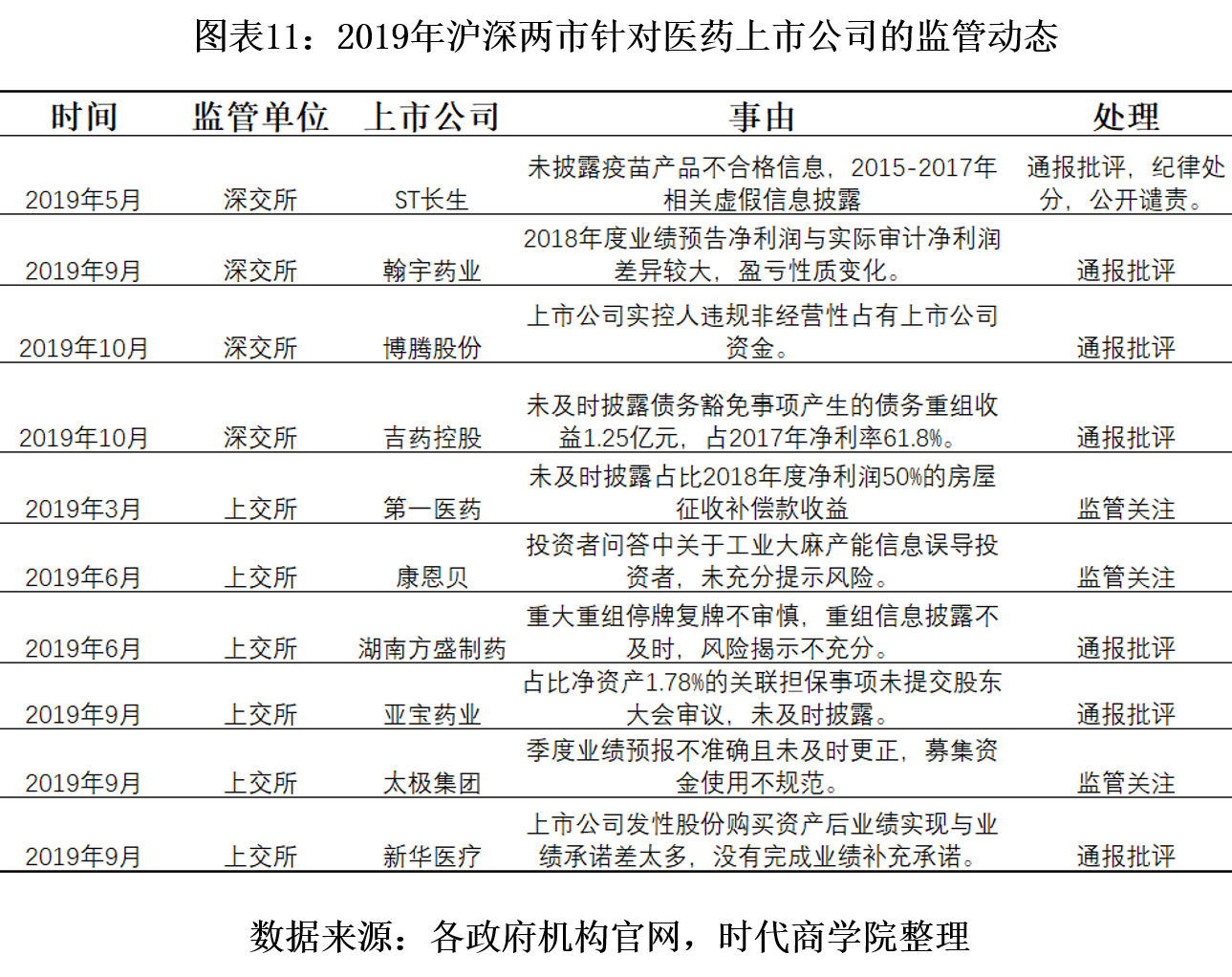
【严正声明】本文(报告)基于已公开的资料信息撰写,文中的信息或所表述的意见均不构成对任何人的投资建议。文章版权归原作者及原出处所有,未经时代商学院授权,任何媒体、网站及微信公众平台不得引用、复制、转载、摘编或以其他任何方式使用上述内容。获得授权转载,仍须注明出处。(联系邮箱:TimesBusiness@163.com)
本网站上的内容(包括但不限于文字、图片及音视频),除转载外,均为时代在线版权所有,未经书面协议授权,禁止转载、链接、转贴或以其他 方式使用。违反上述声明者,本网将追究其相关法律责任。如其他媒体、网站或个人转载使用,请联系本网站丁先生:news@time-weekly.com


