医保目录有望集齐6款抗癌新药,PD-1市场迎来决战时刻
当医保目录迎来新的PD-1玩家,会对国内PD-1市场产生什么影响呢?
PD-1赛道硝烟再起。
 图片来源:pixabay
图片来源:pixabay
近日,国家医保局发布了《2020年国家医保药品目录调整通过形式审查的申报药品名单》,涉及药品多达751种。
其中最引人注目的还是5款PD-1药物,加上去年通过谈判进入国家医保目录的信达生物的PD-1信迪利单抗(商品名:达伯舒),6款在国内获得审批的PD-1药物已经集齐。
根据时代财经了解,PD-1/PD-L1免疫治疗法是一项新型抗癌疗法,治疗肿瘤不用手术、不用化疗,通过药物阻断PD-1/PD-L1通路,激活人体自身的免疫系统攻击肿瘤细胞。
PD-1/PD-L1药物被认为是抗肿瘤治疗的“杀手锏”。但免疫疗法虽好,高昂的治疗费用却让人望而却步。
在没有进入医保目录前,每位患者一年的PD-1药物治疗费用约为10万-30万元。根据IMS数据,2018年全球PD-1抗体药物销售规模约为142亿美元,而国内销售额仅为643.75万美元。
“纳入医保以后,势必会覆盖更多人群,目前除了北上广等一些特别发达的地区外,大多数地区患者无法承受昂贵的费用。”中国抗癌协会肿瘤人工智能专委会委员鲜鹏9月22日接受时代财经采访时表示。
目前,纳入初审目录的PD-1包括百时美施贵宝的纳武利尤单抗(Opdivo)、默沙东的帕博利珠单抗(Keytruda)、君实生物的特瑞普利单抗(商品名:拓益)、百济神州的替雷利珠单抗(商品名:百泽安)、恒瑞医药的卡瑞利珠单抗(商品名:艾瑞卡)。当医保目录迎来新玩家,会对国内PD-1市场产生什么影响呢?
国产PD-1哪家强
截至目前,仅有4种国产PD-1药物在国内获批上市。
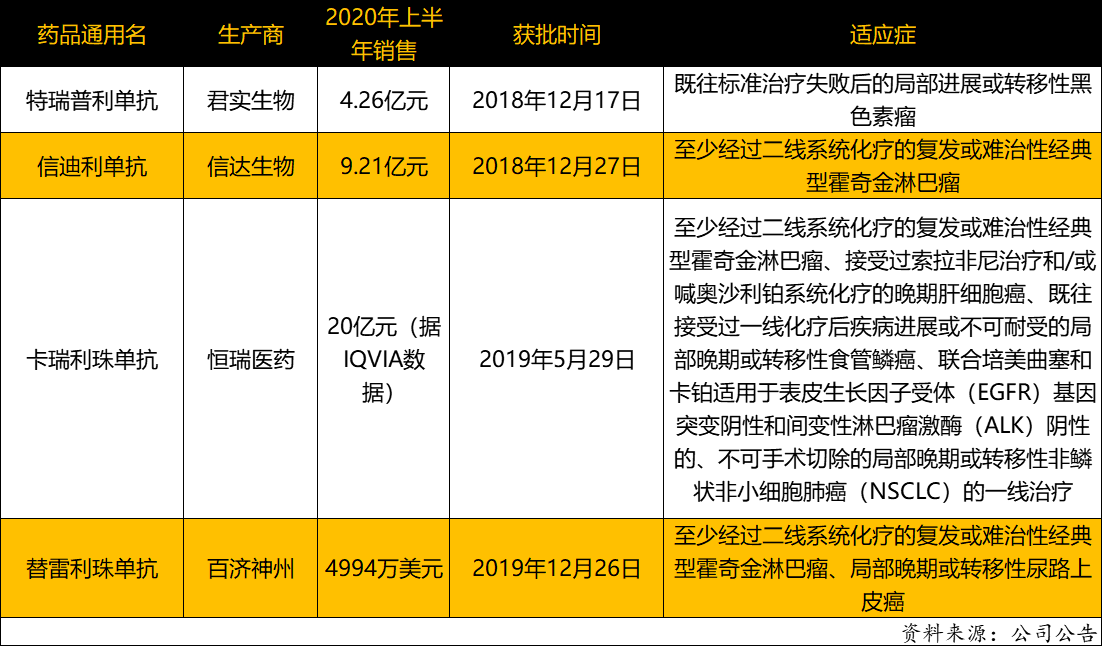
2018年12月17日,君实生物突围,特瑞普利单抗成为第一款获批的国产PD-1单抗,用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。
主要对手信达生物并没有落后太多,10天后(2018年12月27日)信迪利也成功出线,用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的患者。
虽然在上市速度上稍稍落后,但2019年信迪利单抗却率先进入了国家医保目录,也逐渐拉大了和特瑞普利之间的身位。
根据2020半年报,特瑞普利上半年销售额为4.26亿元,信迪利同期卖了9.21亿元。从2019年数据来看,特瑞普利也要稍逊一筹,销售额为7.74亿元,信迪利为10.16亿元。
医保支付并不是导致两者销售差距的唯一因素。
根据弗若斯特沙利文分析,2019 年中国黑色素瘤新发病人数仅为7563人,发病率较低。2019 年新发黑色素瘤病人中,既往标准治疗失败后的局部进展或转移性黑色素瘤患者仅2400人。
这也意味着,目前特瑞普利的销售市场非常有限。
而信迪利的唯一适应症是经典型霍奇金淋巴瘤,淋巴瘤是近年来发病人数增长最快的瘤种之一,尽管霍奇金淋巴瘤仅占淋巴瘤的10%,但根据研究咨询公司GlobalData的数据,2024年霍奇金淋巴瘤治疗市场将达到14亿美元。
 图片来源:时代财经制图
图片来源:时代财经制图
销售成绩最好的国产PD-1药物则是恒瑞医药的卡瑞利珠单抗。
卡瑞利珠于2019年5月获批,虽然时间上晚于特瑞普利和信迪利,但卡瑞利珠是唯一拥有非小细胞肺癌、肝癌等大瘤种适应症的国产PD-1。根据IQVIA的数据,2020年上半年,卡瑞利珠的销售额在20亿元规模左右。
另外一款国产PD-1药物是百济神州的替雷利珠单抗,目前获批的适应症有两个,分别是至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤和局部晚期或转移性尿路上皮癌。
替雷利珠上市时间最晚,但却是信迪利和特瑞普利最有潜力的竞争对手。2019年12月替雷利珠才正式获批,真正实现商业化的时间在2020年3月初。根据百济神州的半年报,替雷利珠约4个月的时间里实现4994万美元(约合3.39亿元)销售收入。
王者“KO”药加入战局
从国际市场看,“K药”Keytruda和“O药”Opdivo的地位无可撼动。
2019年,Keytruda和Opdivo在全球分别“吸金”110.84亿美元和72.04亿美元。Keytruda已经挤进了全球销售榜单TOP10,有预测认为,Keytruda可能会成为默沙东史上最畅销的药物,并在2026年取代艾伯维的阿达木单抗(修美乐)成为新一代“药王”。
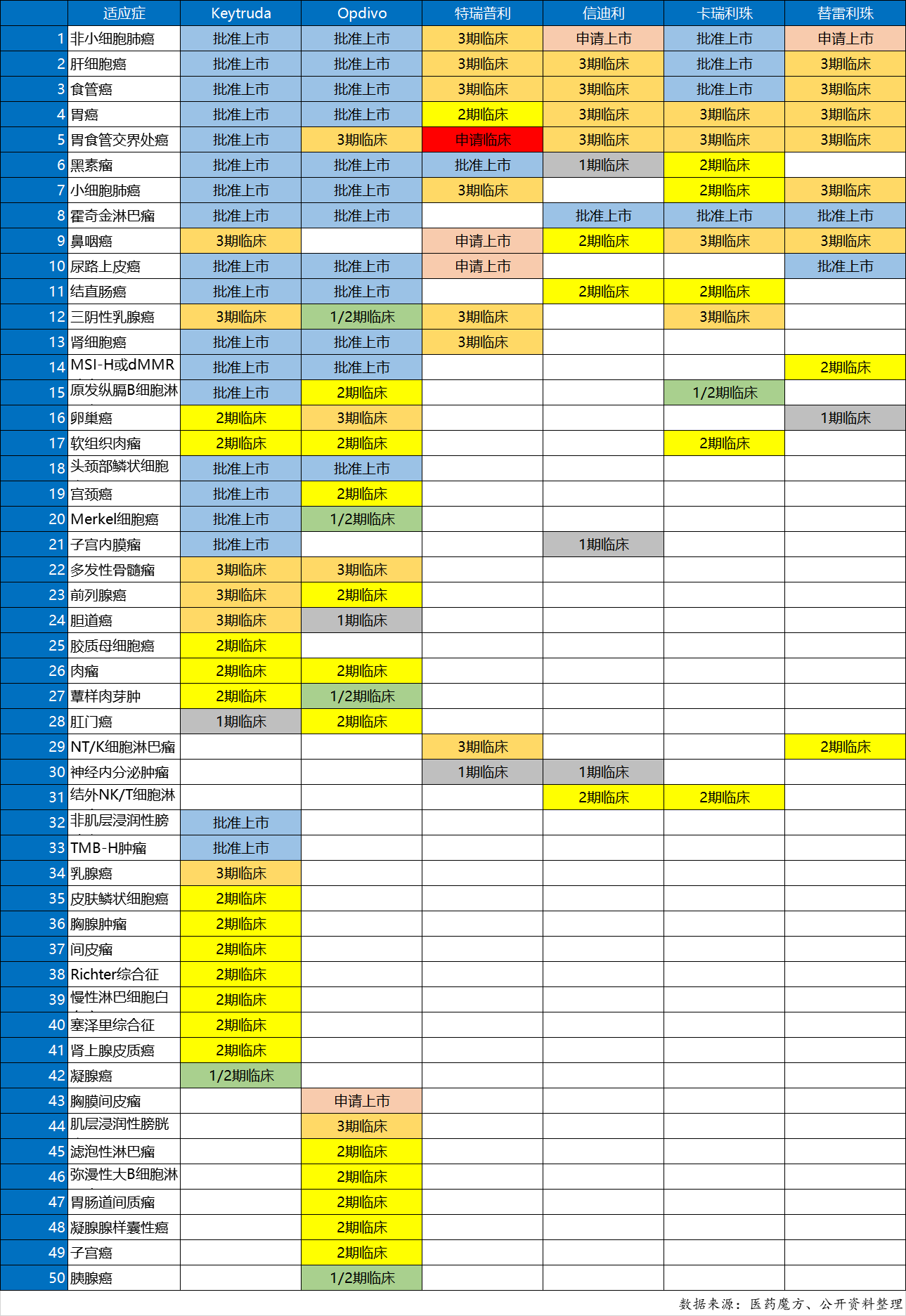
Keytruda和Opdivo的主要优势在于其广泛的适应症。Keytruda以19个适应症领跑全球,Opdivo紧随其后,收获了12个适应症,其中囊括了肺癌、肝癌、胃癌等常见癌种,“秒杀”其他竞争对手。
 图片来源:时代财经制图
图片来源:时代财经制图
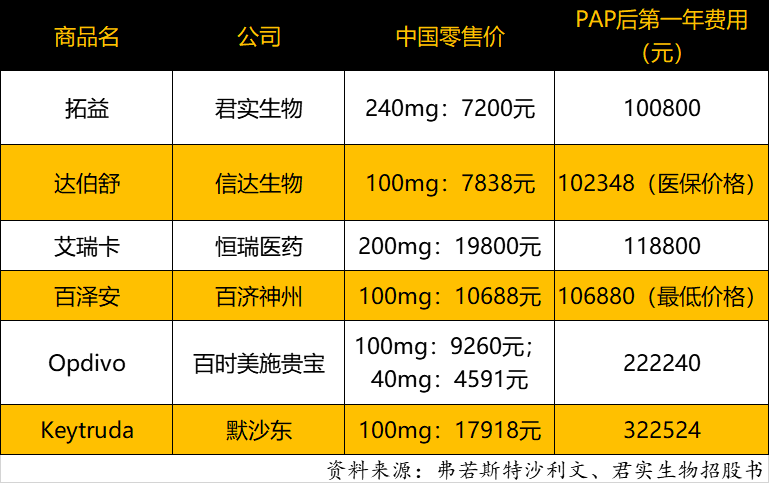
与“KO”相比,价格几乎是国产PD-1药物的唯一优势。
根据弗若斯特沙利文报告,国产PD-1注射剂PAP(患者援助计划或慈善赠药)后一年的费用均在10万元左右,最贵的卡瑞利珠PAP后一年费用也仅为11.8万元。而Keytruda和Opdivo一年的费用分别为32.25万元和22.22万元。
 图片来源:时代财经制图
图片来源:时代财经制图
如果Keytruda和Opdivo愿意“自降身价”进入医保目录,会对国产PD-1造成什么冲击?
鲜鹏指出,Keytruda和Opdivo在中国获批的适应症并不多,而只有用于国内批准的适应症的治疗费用才能被划入医保范围。
在中国,Keytruda 获批的适应症包括黑色素瘤、非小细胞肺癌和食道癌,Opdivo获批的适应症包括非小细胞肺癌、头颈部鳞癌和胃或胃食管连接部腺癌。
从适应症数量上看,“KO”的优势并不明显。但需要指出的是,Keytruda拥有国内唯一一个PD-1单药一线疗法。一线疗法指的是诊断后的首轮治疗,通常只有在一线疗法没有起效时,才会选择二、三线疗法。
不过鲜鹏认为,即使“KO”最终进入医保目录,国产PD-1依然可以保持一定的价格优势。“在进入医保以后,药物价格会有一个较大幅度的下降,但与国产药对比的话,(进口药)的价格估计还是会高出50%以上。”
后来者还有机会吗?
PD-1俨然成了生物药企“标配”。
根据《自然》(Nature)数据,截至2019年8月,全球范围内共有102个候选药物在针对PD-1靶点进行临床试验。
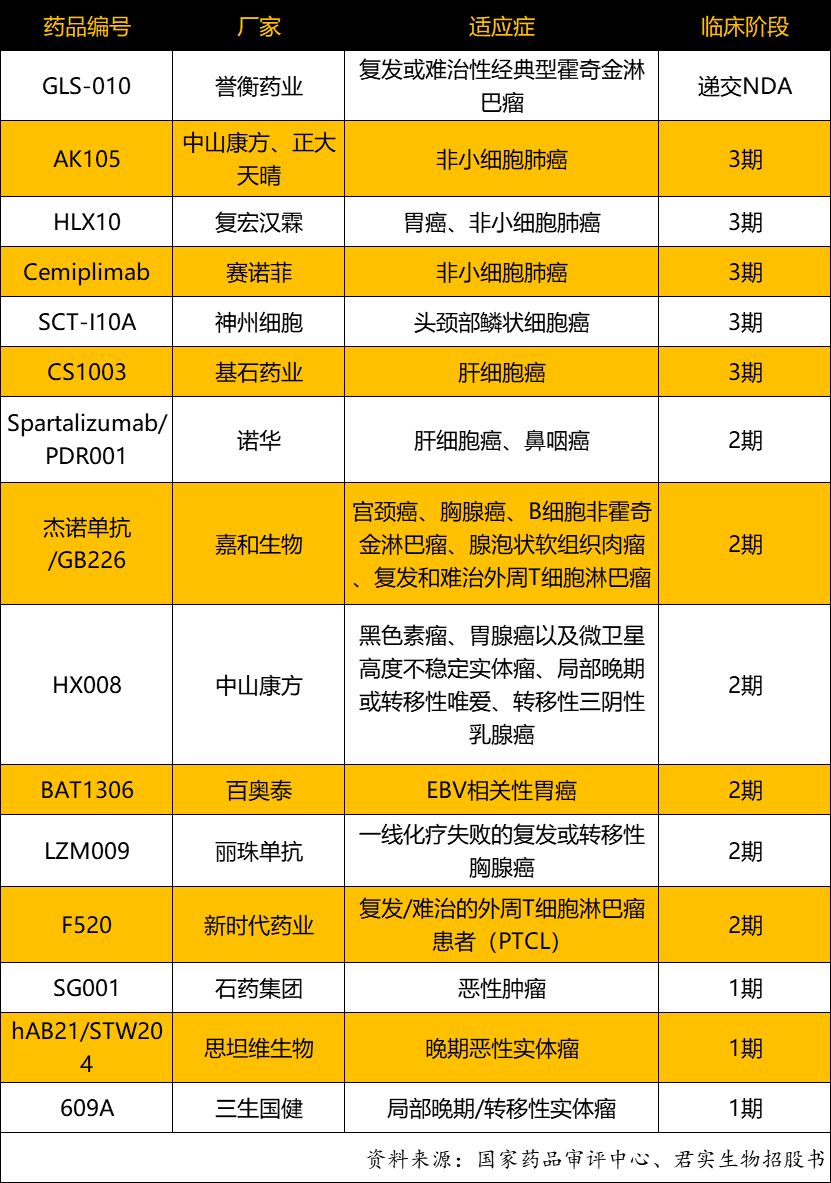
根据君实生物招股书,截至2020年3月31日,除已上市的产品外,中国市场还有15款处于临床或上市申请阶段的PD-1单克隆抗体,全国包括神州细胞、百奥泰、三生国健等知名的创新生物药企。
 图片来源:时代财经制图
图片来源:时代财经制图
据医药魔方报道,在9月19日举办的CSCO学术年会,国内著名肿瘤学教授吴一龙向审评员提问,“目前国内开展PD-1/L1临床试验研究的项目那么多,当已经批准的PD-1/L1达到一定数量,CDE是否会从监管的角度设定一个批准数量?而后申报的项目就不再批准?”
CDE化药临床一部高级审评员夏琳对此回应表示,一方面,早期批准的PD-1多数是附条件批准,假如后续的产品没有出现疗效显著上升的情况下,原则上对同一个适应症不采取附条件批准;另一方面,以NSCLC(非小细胞肺癌)为例,先去批准的PD-1的标准多数是单药对比化疗,而随着越来越多的国产PD-1获批,NSCLC的治疗标准就应该提高到PD-1+化疗,临床设计的对照标准将不再是对照化疗,而是与PD-1+化疗进行对比。
换句话说,虽然CDE不会对PD-1药物批准数量设限,但是审评标准会越来越高。
那么在已有6种PD-1获批的情况下,错失了先机的其他药企还有机会吗?
鲜鹏指出,目前很多国产PD-1在中国的临床试验都是采用了和靶向药物联用的方案。和靶向药物或者化疗药物的联用也可能成为国产PD-1新的突破方向。
时代财经查询国家药物审评中心数据发现,国内目前至少有67项针对PD-1的临床试验项目正在进行,其中有27项为联合用药试验。
本网站上的内容(包括但不限于文字、图片及音视频),除转载外,均为时代在线版权所有,未经书面协议授权,禁止转载、链接、转贴或以其他 方式使用。违反上述声明者,本网将追究其相关法律责任。如其他媒体、网站或个人转载使用,请联系本网站丁先生:news@time-weekly.com






